Manfaat elektrolisis dalam kehidupan sehari hari
Manfaat Elektrolisis dalam kehidupan sehari hari
ELEKTROLISIS
Sel Elektrolisis adalah sel
yang menggunakan arus listrik untuk menghasilkan reaksi redoks yang diinginkan
dan digunakan secara luas di dalam masyarakat kita. Baterai aki yang dapat
diisi ulang merupakan salah satu contoh aplikasi sel elektrolisis dalam kehidupan
sehari-hari. Baterai aki yang sedang diisi kembali (recharge) mengubah
energi listrik yang diberikan menjadi produk berupa bahan kimia yang
diinginkan. Air, H2O, dapat diuraikan dengan menggunakan listrik
dalam sel elektrolisis. Proses ini akan mengurai air menjadi unsur-unsur
pembentuknya. Reaksi yang terjadi adalah sebagai berikut :
2 H2O(l)
——> 2 H2(g) + O2(g)
Rangkaian sel elektrolisis hampir menyerupai sel volta. Yang membedakan sel elektrolisis dari
sel volta
adalah, pada sel elektrolisis, komponen voltmeter diganti
dengan sumber
arus (umumnya baterai).
Larutan atau lelehan yang ingin dielektrolisis, ditempatkan dalam suatu wadah.
Selanjutnya, elektroda dicelupkan ke dalam larutan maupun lelehan elektrolit
yang ingin dielektrolisis. Elektroda yang digunakan umumnya merupakan elektroda
inert, seperti Grafit (C), Platina (Pt), dan Emas (Au). Elektroda berperan
sebagai tempat berlangsungnya reaksi. Reaksi reduksi berlangsung di katoda, sedangkan reaksi oksidasi berlangsung
di anoda. Kutub negatif sumber arus mengarah pada
katoda dan kutub positif sumber arus tentunya mengarah pada anoda.
Akibatnya, katoda bermuatan
negatif dan menarik kation-kation yang akan tereduksi menjadi endapan logam. Sebaliknya, anoda bermuatan positif dan
menarik anion-anion
yang akan teroksidasi menjadi
gas. Sebagai contoh, berikut ini adalah reaksi elektrolisis lelehan garam NaCl
(yang dikenal dengan istilah sel Downs) :
Katoda
(-)
: 2 Na+(l) + 2 e- ——> 2
Na(s) ………………........................ (1)
Anoda (+)
: 2 Cl-(l) Cl2(g) + 2 e-
………………...................................... (2)
Reaksi
sel
: 2 Na+(l) + 2 Cl-(l) ——>
2 Na(s) + Cl2(g) ……………….. [(1) + (2)]
Reaksi elektrolisis lelehan garam NaCl menghasilkan
endapan logam natrium di katoda dan gelembung gas Cl2 di anoda.
Beberapa aplikasi elektrolisis
antara lain :
Elektroplatting
Elektroplatting adalah aplikasi
elektrolisis pada pelapisan suatu logam atas logam yang lain. Teknik ini bisa
dipakai untuk memperbaiki penampakan dan daya tahan suatu logam. Contohnya,
suatu lapisan tipis logam chromium pada bemper baja mobil untuk membuatnya menarik
dan melindunginya dari karat. Pelapisan emas dan perak dilakukan pada barang-barang
perhiasan yang berasal dari bahan-bahan logam yang murah. Berbagai
lapisan-lapisan tipis logam tersebut ketebalannya berkisar antara 0,03 s/d 0,05
mm.
·
Pembuatan Aluminium
Bauksit adalah biji aluminium yang
mengandung Al2O3-. Untuk mendapatkan
aluminium, bijih tersebut dimurnikan dan Al2O3 nya
dilarutkan dan didisosiasikan dalam larutan elektrolit. Pada katoda, ion-ion
aluminium direduksi menghasilkan logam yang terbentuk sebagai lapisan tipis
dibagian bawah wadah elektrolit. Pada anoda yang terbuat dari karbon, ion
oksida teroksidasi menghasilkan O2 bebas.
Reaksinya
adalah :
Al3+
+ 3e- → Al(l) (katoda)
2O2-
→ O2(g) + 4 e- (anoda)
4Al3+
+ 6O2- → 4Al(l) + 3O2(g) (total)
·
Pembuatan Magnesium
Sumber utama magnesium adalah air
laut. Mg2+ mempunyai kelimpahan terbesar ketiga dalam laut,
kalahannya oleh ion natrium dan ion klorida. Untuk memperoleh magnesium, Mg(OH)2
diendapkan dari air laut. Pemisahan itu dilakukan dengan cara filtrasi dan lalu
dilarutkan dalam asam hidroklorit.
Mg(OH)2 + 2HCl → MgCl2 + 2H2O
Larutan MgCl2 diuapkan dan menghasilkan
MgCl2 padat yang lalu dilelehkan dan akhirnya dielektrolisa.
Magnesium bebas akan diendapkan pada katoda dan gas klorin dihasilkan pada
anoda.
MgCl2(l) → Mg(l) + Cl2(g)
·
Penyulingan Tembaga
Tembaga tidak murni dipakai sebagai
elektroda sebagai anoda pada sel elektrolisis yang mengandung larutan tembaga
sulfat dan asam sulfat (sebagai elektrolit). Katoda pada sistem ini adalah
tembaga dengan kemurnian tinggi. Jika selnya dijalankan pada tegangan yang
diperlukan, hanya tembaga dan pengotornya yang lebih mudah teroksidasi daripada
tembaga, seng dan besi yang larut disekitar anoda. Logam-logam yang kurang
aktif akan runtuh dan mengendap dibagian dasar wadah. Pada katoda, ion tembaga
direduksi tetapi ion seng dan ion besi tertinggal dilarutan karena lebih sukar
tereduksi dari pada tembaga. Secara pelan-pelan tembaga anoda terlarut dan
tembaga katoda makin tumbuh. Suatu saat tembaga akan mempunyai kemurnian 99,95%.
Kotoran yang terkumpul dibagian bawah biasanya disebut sebgai anoda, dapat
dipindahkan secara periodik dan nilai perak, emas dan platina dapat pula
dihitung untuk memperoleh total efisiensi pelaksanaan proses penyulingan.
·
Elektrolisis Brine
Brine (=’air asin’) adalah larutan
natrium klorida jenuh. Pada katoda, air lebih mudah direduksi daripada ion
natrium dan gas H2 akan terbentuk. Reaksi :
2e- + 2H2O → H2(g) +
2OH-(aq)
Walaupun air lebih mudah teroksidasi daripada ion
klorida, namun seperti telah disebut bahwa ada faktor-faktor yang kompleks yang
mempengaruhi sehingga yang teroksidasi adalah ion klorida.
Manfaat elektrolisis dalam kehidupan sehari- hari
Manfaat elektrolisis dalam kehidupan sehari- hari
Pembuatan Beberapa Bahan Kimia
Beberapa bahan kimia seperti logam alkali dan alkali tanah aluminium,
gas hidrogen, gas oksigen, gas klorin, dan natrium hidroksida dibuat
secara elektrolisis.
Contoh : Pembuatan logam natrium dengan mengelektrolisis lelehan NaCl yang dicampur dengan CaCl2
NaCl(l) → Na+(l) + Cl-(l)
Katoda :
|
Na+(l) + e-
|
→
|
Na(l)
|
(x
2)
|
Anoda :
|
2Cl-(l)
|
→
|
Cl2(g) + 2e-
|
|
2Na+(l) + 2Cl-(l)
|
→
|
2Na(l) + Cl2(g)
|
Natrium cair yang terbentuk di katoda mengapung di atas cairan NaCl, kemudian dikumpulkan pada kolektor.
Pemurnian Logam
Pada pengolahan tembaga dari bijih kalkopirit diperoleh tembaga yang
masih tercampur dengan sedikit perak, emas, dan platina. Untuk beberapa
keperluan dibutuhkan tembaga murni, misalnya untuk membuat kabel.
Tembaga yang tidak murni dipisahkan dari zat pengotornya dengan
elektrolisis.
Tembaga yang tidak murni dipasang sebagai anoda dan tembaga murni dipasang sebagai katoda dalam elektrolit larutan CuSO4 tembaga di anoda akan teroksidasi menjadi Cu2+ selanjutnya Cu2+ direduksi di katoda.
Anoda
|
:
|
Cu(s)
|
→
|
Cu2+(aq) +2e-
|
Katoda
|
:
|
Cu2+(aq) + 2e-
|
→
|
Cl2(g) + 2e-
|
Cu(s)
|
→
|
Cu(s)
|
||
anoda
|
Katoda
|
Dengan demikian tembaga di anoda pindah ke katoda sehingga anode semakin
habis dan katoda semakin bertambah besar. Logam emas, perak, dan
platina terdapat pada lumpur anoda sebagai hasil samping pada pemurnian
tembaga.
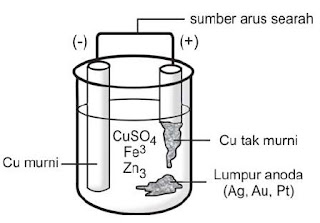 |
| Gambar 1. Pemurnian tembaga. |
Suatu produk dari logam agar terlindungi dari korosi (perkaratan) dan
terlihat lebih menarik seringkali dilapisi dengan lapisan tipis logam
lain yang lebih tahan korosi dan mengkilat. Salah satu cara melapisi
atau menyepuh adalah dengan elektrolisis. Benda yang akan dilapisi
dipasang sebagai katoda dan potongan logam penyepuh dipasang sebagai
anoda yang dibenamkan dalam larutan garam dari logam penyepuh dan
dihubungkan dengan sumber arus searah.
Contoh : untuk melapisi sendok garpu yang terbuat dari baja dengan
perak, maka garpu dipasang sebagai katoda dan logam perak dipasang
sebagai anoda, dengan elektrolit larutan AgNO3. Seperti terlihat pada gambar 2.
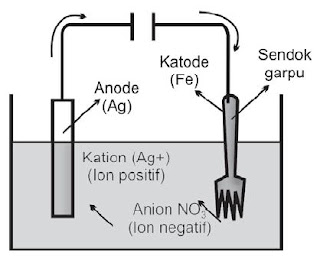 |
| Gambar 2. Pelapisan sendok dengan logam perak. |
Logam perak pada anoda teroksidasi menjadi Ag+ kemudian direduksi menjadi Ag pada katoda atau garpu. Dengan demikian garpu terlapisi. oleh logam perak.
Anoda
|
:
|
Ag(s)
|
→
|
Ag+(aq)+ e-
|
Katoda
|
:
|
Ag+(aq) + e-
|
→
|
Ag (s)
|
Ag(s)
|
→
|
Ag(s)
|
||
anoda
|
Katoda
|
Terima kasih
Lihat juga:
